साइट्रिक एसिड क्या है? (Citric acid kya hai) इसके गुण, सूत्र, संरचना, उपयोग (साइट्रिक अमल के उपयोग) और तैयार करने की विधि (साइट्रिक अमल बिनने की विधि) पर आज इस लेख में चर्चा की जाएगी। साइट्रिक एसिड साइट्रस फलों और अन्य साइट्रस फलों से प्राप्त किया जाता है। यह औद्योगिक स्तर पर उपयोग किया जाने वाला एक महत्वपूर्ण पदार्थ है। इसका उपयोग कई उत्पादों के संश्लेषण में किया जाता है।
2018 में वैश्विक उत्पादन 2,000,000 टन से अधिक था। इस मात्रा का 50% से अधिक उत्पादन चीन में किया गया था। 50% से अधिक पेय पदार्थों में अम्लता नियामक के रूप में उपयोग किया जाता था, अन्य खाद्य अनुप्रयोगों में 20%, डिटर्जेंट अनुप्रयोगों के लिए 20%, और खाद्य पदार्थों के अलावा अन्य अनुप्रयोगों के लिए 10%, जैसे सौंदर्य प्रसाधन, फार्मास्यूटिकल्स और रासायनिक उद्योग में। साइट्रिक एसिड क्या है?
साइट्रिक एसिड क्या है?
साइट्रिक अम्ल एक कमजोर कार्बनिक अम्ल है। इसका रासायनिक सूत्र C6H8O7 है। साइट्रिक एसिड का आणविक भार 192.123 g/mol (निर्जल) और 210.14 g/mol है (monohydrate). साइट्रिक एसिड और इसके लवण नींबू, संतरे और कई खट्टे फलों में पाए जाते हैं। यह पशु उत्पादों में भी कम मात्रा में पाया जाता है। नींबू के रस में 6 से 7 प्रतिशत साइट्रिक एसिड होता है।
साइट्रिक एसिड बड़े समस्थानिक प्रिज्मों के क्रिस्टल बनाता है। यह पानी और अल्कोहल में घुल जाता है। लेकिन यह ईथर में बहुत कम घुलता है। यह वास्तव में 2-हाइड्रॉक्सी-प्रोपेन 1:2:3 ट्राइकार्बोसिलिक एसिड है। साइट्रिक एसिड को पहली बार 1784 में रसायनज्ञ कार्ल विल्हेम शील द्वारा संश्लेषित किया गया था।
साइट्रिक एसिड की संरचना.. साइट्रिक एसिड की संरचना एक एककोशिकीय क्रिस्टल संरचना है। एक साइट्रिक एसिड अणु तीन कार्बोक्जिलिक एसिड समूहों और एक हाइड्रॉक्सिल समूह से बना होता है। चारों समूह 5 कार्बन श्रृंखलाओं से जुड़े हुए हैं। अणु में कार्बोक्जिलिक समूह में एक समतलीय संरचना होती है। हालांकि मुख्य श्रृंखला में 3 टेट्राहेड्रल कार्बन भी होते हैं।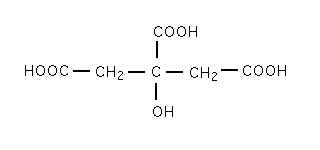
सिट्रिक एसिड के भौतिक व रासायनिक गुण
- यह एक दुर्बल कार्बनिक अम्ल है
- इसका रासायनिक सूत्र C₆H₈O₇ व अणुभार 192.123 g /mol (anhydrous) ), 210.14 g / mol (मोनोहाइड्रेट) होता है।
- यह गंधरहित व क्रिस्टलीय सफेद ठोस होता है।
- इसका घनत्व 1.665 g / cm (anhydrous) और 1.542 g / cm ( मोनोहाइड्रेट) होता है।
- इसका गलनांक 156 ° C (313 ° F; 429 K) होता है।
- इसका क्वथनांक 310 ° C (anhydrous) और 175 ° C (monohydrate) होता है।
- यह जल, एल्कोहल,एसीटोन, शराब , ईथर , एथिल एसीटेट , DMSO,C6H6, CHCl 3, CS2, में घुलनशील होता है। यह ईथर में कम घुलनशील होता है।
- इसकी संरचना एककोशकीय क्रिस्टल संरचना होती है।
- सिट्रिक अम्ल बड़े-बड़े समचतुर्भुजीय प्रिज्म का क्रिस्टल बनाता है।
- सिट्रिक अम्ल के क्रिस्टल में क्रिस्टल जल रहता है जिसे 130° C पर गर्म करने पर यह अजल हो जाता है।
- यह त्रिक्षारक अम्ल है और तीन श्रेणियों का लवण बनाता है। कुछ लवण जल में विलेय, कुछ अल्प विलेय और कुछ अविलेय होते हैं।
- सिट्रिक एसिड निर्जल (anhydrous) तथा मोनोहाइड्रेट के रूप में मौजूद होता है। निर्जल (anhydrous) सिट्रिक अम्ल गर्म पानी से क्रिस्टलीकृत होता है। जबकि मोनोहाइड्रेट सिट्रिक अम्ल ठंडे पानी से क्रिस्टलीकृत होता है।
- मोनोहाइड्रेट सिट्रिक अम्ल को लगभग 78 डिग्री सेल्सियस पर निर्जल (anhydrous) रूप में परिवर्तित किया जा सकता है।
- यह 175 डिग्री सेल्सियस से ऊपर कार्बन डाइऑक्साइड के नुकसान के साथ विघटित हो जाता है।
- सिट्रिक अम्ल का pH 3 से 6 होता है। यह pH रेंज इसकी सांद्रता पर निर्भर करती है। सिट्रिक एसिड के 1 mm विलयन का pH लगभग 3.2 होगा।
यह एक त्रि-चक्रीय अम्ल है और लवणों के तीन वर्ग बनाता है। कुछ पानी में घुलनशील हैं, कुछ अघुलनशील हैं और कुछ अघुलनशील हैं।
साइट्रिक एसिड निर्जल और मोनोहाइड्रेट के रूप में मौजूद होता है। निर्जल साइट्रिक अम्ल गर्म पानी से क्रिस्टलीकृत होता है। जबकि मोनोहाइड्रेट साइट्रिक एसिड ठंडे पानी से क्रिस्टलीकृत होता है।
मोनोहाइड्रेट साइट्रिक एसिड को लगभग 78 डिग्री सेल्सियस पर निर्जल रूप में परिवर्तित किया जा सकता है।
यह 175 डिग्री सेल्सियस से ऊपर कार्बन डाइऑक्साइड के नुकसान के साथ विघटित होता है।
साइट्रिक अम्ल का पीएच 3 से 6 होता है। यह पीएच सीमा इसकी सांद्रता पर निर्भर करती है। साइट्रिक एसिड के 1 मिमी समाधान का पीएच लगभग 3.2 होगा।
साइट्रिक एसिड का उपयोग पानी को नरम करने के लिए किया जाता है।
साइट्रिक एसिड का उपयोग भोजन और शीतल पेय में खट्टापन जोड़ने के लिए किया जाता है।
साइट्रिक एसिड एक प्राकृतिक संरक्षक है।
जैव रसायन में इसका महत्व इसलिए है क्योंकि यह सभी जीवित जीवों का चयापचय चक्र बनाता है।
यह पर्यावरण को नुकसान पहुंचाए बिना सफाई के काम के लिए उपयुक्त है।
साइट्रिक एसिड का उपयोग सफाई उत्पादों में किया जाता है।
साइट्रिक एसिड का उपयोग पूरक के रूप में किया जाता है। मैग्नीशियम और कैल्शियम जैसे खनिज पूरकों में साइट्रिक एसिड हो सकता है। यह गुर्दे की पथरी के खतरे को कम करता है।
साइट्रिक एसिड का उपयोग दवाओं के निर्माण में किया जाता है। साइट्रिक एसिड वाली दवाएँ लेने से मूत्र में एसिड की मात्रा कम हो जाती है।
भोजन को संरक्षित करने के लिए डिब्बाबंद सामानों और ठंडे पेय पदार्थों में साइट्रिक एसिड का उपयोग किया जाता है।
साइट्रिक एसिड का प्रयोग प्रयोगशाला में अभिकर्मक के रूप में भी किया जाता है।
इसका उपयोग दवा और खाद्य उद्योगों में किया जाता है।
साइट्रिक एसिड का उपयोग रंगाई और रंगाई में किया जाता है।
साइट्रिक एसिड के अन्य उपयोग साइट्रेट्स के बफरिंग गुणों का उपयोग घरेलू क्लीनर और फार्मास्यूटिकल्स में पीएच को नियंत्रित करने के लिए किया जाता है।
अम्लीय रंगों से कपड़ों को रंगने के लिए सफेद सिरके के गंधहीन विकल्प के रूप में साइट्रिक एसिड का उपयोग किया जाता है।
सोडियम साइट्रेट बेनेडिक्ट के अभिकर्मक का एक घटक है, जिसका उपयोग शर्करा को कम करने की गुणात्मक और मात्रात्मक पहचान दोनों के लिए किया जाता है।
स्टेनलेस स्टील के निष्क्रियकरण में साइट्रिक एसिड का उपयोग नाइट्रिक एसिड के विकल्प के रूप में किया जा सकता है।
फोटोग्राफिक फिल्म विकसित करने के लिए एक प्रक्रिया के रूप में साइट्रिक एसिड का उपयोग कम गंध वाले स्टॉप बाथ के रूप में किया जा सकता है। फोटोग्राफिक डेवलपर क्षारीय होते हैं। इसलिए एक हल्के अम्ल का उपयोग उनकी क्रिया को जल्दी से बेअसर करने और रोकने के लिए किया जाता है। लेकिन इस्तेमाल किया जाने वाला एसिटिक एसिड अंधेरे कमरे में एक मजबूत सिरके की गंध छोड़ देता है।
साइट्रिक एसिड/पोटेशियम-सोडियम साइट्रेट का उपयोग रक्त एसिड नियामक के रूप में किया जा सकता है।
शुष्क या पानी में एक केंद्रित विलयन के रूप में साइट्रिक एसिड एक उत्कृष्ट सोल्डरिंग फ्लक्स है। सिलाई के बाद इसे हटा देना चाहिए। क्योंकि यह हल्का संक्षारक होता है। यह गर्म पानी में घुल जाता है और जल्दी से धोया जाता है।
प्राकृतिक घटना और साइट्रिक एसिड का औद्योगिक उत्पादन साइट्रिक एसिड विभिन्न प्रकार के फलों और सब्जियों में मौजूद होता है। (especially in citrus fruits). नींबू और नींबू में एसिड की उच्च सांद्रता होती है। यह इन फलों के सूखे वजन का 8% तक हो सकता है। नींबू के रस में लगभग 47 ग्राम/लीटर साइट्रिक एसिड होता है। साइट्रस फलों में साइट्रिक एसिड की सांद्रता संतरे और अंगूर के लिए 0.005 मोल/एल के बीच होती है। जबकि नींबू और चूने में यह सांद्रता 0.30 मोल/लीटर है।
साइट्रिक एसिड को पहली बार 1784 में रसायनज्ञ कार्ल विल्हेम शील द्वारा अलग किया गया था। उन्होंने इसे नींबू के रस के साथ क्रिस्टलाइज़ करके प्राप्त किया था। औद्योगिक पैमाने पर साइट्रिक एसिड का उत्पादन पहली बार 1890 में इतालवी साइट्रस फल उद्योग के रूप में शुरू हुआ।
जहाँ रस को कैल्शियम साइट्रेट को अवक्षेपित करने के लिए हाइड्रेटेड लाइम (कैल्शियम हाइड्रॉक्साइड) के साथ उपचारित किया गया था। और पतला सल्फ्यूरिक एसिड का उपयोग करके वापस एसिड में परिवर्तित किया गया था। 1893 में सी. वेहमर ने पाया कि पेनिसिलियम मोल्ड चीनी से साइट्रिक एसिड का उत्पादन कर सकता है।
1917 में, अमेरिकी खाद्य रसायनज्ञ जेम्स क्यूरी ने मोल्ड के कुछ उपभेदों की खोज की। दवा कंपनी फाइजर ने दो साल बाद इस तकनीक का उपयोग करके औद्योगिक पैमाने पर इसका उत्पादन शुरू किया। इस तकनीक को बाद में 1929 में सिट्रिक बेल्ज द्वारा पेश किया गया था। वर्तमान में साइट्रिक एसिड का औद्योगिक उत्पादन इसी तकनीक से किया जाता है।
ए. नाइजर के संवर्धनों को साइट्रिक एसिड का उत्पादन करने के लिए सुक्रोज या ग्लूकोज युक्त माध्यम पर सिंचित किया जाता है। चीनी का स्रोत कॉर्नस्टार्च अल्कोहल, शीरा, हाइड्रोलाइज्ड कॉर्न स्टार्च या अन्य सस्ता मीठा घोल है। कैल्सियम साइट्रेट नमक को परिणामी घोल से मोल्ड को छानने के बाद कैल्सियम हाइड्रॉक्साइड के साथ साइट्रिक एसिड को अवक्षेपित करके प्राप्त किया जाता है। जिसमें साइट्रिक एसिड को पतला सल्फ्यूरिक एसिड के साथ उपचारित किया जाता है। जैसे कि साइट्रस फलों के रस से सीधे निष्कर्षण में।
1977 में, लीवर ब्रदर्स को साइट्रिक एसिड के रासायनिक संश्लेषण के लिए एक पेटेंट प्रदान किया गया था। जो उच्च दबाव की स्थिति में एकोनाइट या आइसोसिट्रेट/एलोआइसोसिट्रेट कैल्शियम लवणों से शुरू होता है। यह एक विपरीत, गैर-एंजाइमेटिक क्रेब्स चक्र प्रतिक्रिया के रूप में लगभग मात्रात्मक रूपांतरण में साइट्रिक एसिड का उत्पादन करता है।
सुरक्षा साइट्रिक एक कमजोर अम्ल है। लेकिन इसके संपर्क में आने से मानव शरीर पर प्रतिकूल प्रभाव पड़ सकता है। खाँसी, घरघराहट और सांस की तकलीफ हो सकती है। इसके अत्यधिक सेवन से पेट दर्द और मतली हो सकती है। केंद्रित घोल के संपर्क में आने से त्वचा और आंखों में लालिमा और दर्द हो सकता है। लंबे समय तक या बार-बार उपयोग करने से दांत के तामचीनी का क्षरण हो सकता है।
Translate text instantly with our











